BIOEQUIVALENCIA EN MEDICAMENTOS GENÉRICOS. QUÉ ES?
Existen dos tipos de medicamentos: el innovador y el genérico. El medicamento genérico es creado para ser o tratar de ser igual a un medicamento innovador en cuanto a su dosificación, seguridad, potencia, vía de administración, calidad, características de rendimiento y uso previsto.
Vale recalcar que dentro de los genéricos, existen genéricos puros y genéricos con nombre fantasía. Sin embargo un nombre de fantasía no lo desprende de su naturaleza genérica. Esta táctica de nombres fantasía la han usado algunas empresas de medicamentos genéricos, que tal vez quieren insinuar que no lo son. Sin embargo, esa posición es utópica: por definición, un medicamento que no es innovador lo hace automáticamente un genérico.
Lo que sí es relevante y diferencial entre medicamentos genéricos es si estos están respaldados por pruebas de bioequivalencia clínica. Ya que: un mismo comportamiento farmacocinético es la única garantía para lograr el mismo efecto farmacodinámico.
NORMON ES BIOEQUIVALENCIA REAL
Como introducción presentamos un video producido y publicado por Laboratorios Normon. Productos con bioequivalencia, desde su nacimiento.



PREGUNTAS FRECUENTES - BIOEQUIVALENCIA
-
Con pruebas de bioequivalencia clínica.
Así es como un medicamento genérico demuestra que funciona de la misma manera y proporciona el mismo beneficio clínico que su versión innovadora. En otras palabras, usted puede sustituir su medicamento innovador con un medicamento genérico bioequivalente sin ninguna duda.
Las pruebas de bioequivalencia son usualmente costosas, de difícil acceso y rondando los cientos de miles de dólares por producto. Puede explicar que quizá no cualquier fabricante puede hacerlas, y/o no para todos sus productos.
Fuente: U.S. FOOD AND DRUG ADMINISTRATION. FDA: Medicamentos Genéricos: Preguntas y Respuestas
Un medicamento que no es original, y no tiene pruebas de equivalencia, se le considera una “copia”.
-
No.
En Costa Rica, no todos los medicamentos genéricos son bioequivalentes ni intercambiables. Aunque la oferta de genéricos (puros y con nombre fantasía) en las farmacias es sumamente amplia, solo una fracción menor cuenta con estudios clínicos de bioequivalencia que demuestren que su comportamiento en el organismo es equivalente al del medicamento original.
La mayoría de los medicamentos genéricos —tanto los llamados genéricos puros como los de nombre comercial o fantasía— no disponen de dichas pruebas. Por eso, deben considerarse copias - no cuentan con garantía de intercambiabilidad terapéutica.
Actualmente, sólo unos pocos laboratorios de origen internacional son reconocidos por ofrecer portafolios 100% bioequivalentes, desde su lanzamiento. Entre ellos destacan dos laboratorios españoles, uno suizo, uno canadiense y uno alemán. Las agencias regulatorias de esos países no los dejan comercializar hasta que presenten estas pruebas.
Laboratorios Normon forma parte de este grupo selecto, ofreciendo productos con bioequivalencia comprobada, fabricados bajo las más altas normas de calidad de la OMS y la Unión Europea, y a precios competitivos, incluso con precios más atractivos que genéricos con nombre fantasía y sin pruebas de bioequivalencia.
Por su parte, el Ministerio de Salud de Costa Rica ha avanzado significativamente en esta materia, fortaleciendo su marco regulatorio. Hoy en día, muchos medicamentos de uso común ya requieren presentar estudios de bioequivalencia para obtener o renovar su registro sanitario. Puede consultar la lista oficial publicada por la autoridad sanitaria en el siguiente enlace:
Ministerio de Salud - Bioequivalencia Terapéutica -
Las consideraciones pueden ser muchas, sin embargo existen algunas básicas que deben de respetarse siempre.
Los estudios se basan en el principio de que en una misma persona, si un mismo principio activo contenido en dos medicamentos similares (la especialidad genérica y la de referencia) se absorbe en la misma cantidad y velocidad en sangre, se hallará en el lugar donde ejerce la acción en una concentración similar ejerciendo entonces un efecto terapéutico también similar.
Aparte de las pruebas clínicas con personas sanas (in vivo), se complementan con otro tipo de pruebas químicas de laboratorio llamadas “pruebas de disolución” (in situ). Sin embargo estas pruebas “in situ” son tan solo complementarias, son menos complejas, y por sí solas no pueden determinar que un medicamento es bioequivalente.
-
Sí.
Cualquier medicamento genérico con pruebas de bioequivalencia efectivas contra un medicamento innovador como modelo, tiene los mismos efectos en el cuerpo que ese medicamento de marca. Es igual en cuanto a su dosificación, seguridad, efectividad, potencia, estabilidad y calidad, así como en la forma en que se toma y la forma en que se debe utilizar.
Los medicamentos genéricos bioequivalentes utilizan los mismos ingredientes activos que los medicamentos de marca y funcionan de la misma manera, por lo que tienen los mismos riesgos y beneficios que los medicamentos de marca.
-
En Costa Rica, el Ministerio de Salud. En el siguiente vínculo podrá encontrar la lista de moléculas que requieren de pruebas de bioequivalencia para otorgar o renovar su registro sanitario: Ministerio Salud CR - Listado de productos de referencia
Por otro lado, en el caso del origen de Laboratorios Normon, la encargada es la Agencia Española de Medicamentos y Productos Sanitarios del Ministerio de Sanidad, Política Social e Igualdad. Esta, es una agencia regulatoria que cumple con estándares mundiales de regulación de la máxima talla a nivel mundial, de acuerdo a la OMS.
En España, todos los medicamentos de uso humano de fabricación industrial deben contar con los requisitos establecidos de calidad, pruebas completas de bioequivalencia (in vivo e in situ), así como pruebas de seguridad y eficacia, para obtener la autorización de comercialización de la Agencia.
La Agencia, en el proceso de autorización de comercialización de un medicamento genérico exige los mismos requisitos que para un medicamento original excepto los estudios preclínicos y clínicos del principio activo (que están ya realizados para el medicamento original de marca).
-
No, los genéricos bioequivalentes producen los mismos efectos y en el mismo período de tiempo que el medicamento original de marca. Para ello eben demostrar su bioequivalencia terapéutica en comparación con el medicamento original.
Un medicamento genérico (con o sin marca fantasía) sin pruebas de bioequivalencia pueden tener respuestas diferentes al original como tardar más tiempo en surtir efecto. Fuente: Gobierno de España. Preguntas frecuentes de medicamentos genéricos.
-
Si, son intercambiables. Para ser autorizados por la Agencia Española de Medicamentos y Productos Sanitarios, deben demostrar su bioequivalencia terapéutica con el medicamento original de marca que le sirve de referencia, por medio de estudios de biodisponibilidad.
-
Siempre habrá un nivel leve de variabilidad natural que carece de importancia médica, relacionada a factores como: diferencias genéticas entre pacientes, estado fisiológico, interacciones con otros medicamentos y estilo de vida.
Sin embargo es gracias a las pruebas de bioequivalencia que se pueden garantizar que dos medicamentos en su misma versión (el de marca y un genérico) son productos iguales que van a causar el mismo efecto terapéutico. Sin esta garantía, la variabilidad sería aún mayor que la descrita en el párrafo anterior y esa diferencia sí tomaría relevancia médica. Es por eso que los profesionales en salud y pacientes deben prestar atención a este tema.Fuente: Davit et al. Comparing generic and innovator drugs: a review of 12 years of bioequivalence data from the United States Food and Drug Administration (“Comparación de medicamentos genéricos e innovadores: una revisión de 12 años de datos de bioequivalencia de la Administración de Alimentos y Medicamentos de los Estados Unidos”). Ann Pharmacother. 2009; 43(10):1583-97.
-
La razón por la que los medicamentos genéricos cuestan menos que los innovadores es principalmente económica y estructural dentro de la industria farmacéutica.
1. Costos de desarrollo e investigación
Los medicamentos innovadores (también llamados de marca o de referencia) requieren:
Entre 10 a 15 años de investigación y ensayos clínicos.
Una inversión promedio de 1.5 a 2.5 mil millones de dólares.
Altos costos en patentes, estudios toxicológicos, farmacocinéticos, farmacodinámicos y de eficacia clínica.
Estos costos deben recuperarse durante el período de exclusividad de patente (20 años). Por eso, las farmacéuticas innovadoras fijan precios altos: no sólo para cubrir el costo del medicamento, sino el de todos los proyectos fallidos previos.
En cambio, los genéricos se desarrollan cuando la patente expira. No necesitan repetir los estudios clínicos de eficacia y seguridad —solo deben demostrar bioequivalencia con el innovador—, lo que reduce drásticamente su costo de entrada al mercado.
2. Ausencia de costos de marketing y posicionamiento
Las compañías innovadoras invierten enormes sumas en:
Promoción médica y campañas publicitarias.
Formación de fuerza de ventas y médicos líderes de opinión.
Distribución inicial y posicionamiento global.
Los fabricantes de genéricos se benefician del conocimiento ya creado: el médico y el paciente ya reconocen el principio activo.
Por eso, sus costos de marketing son mínimos.3. Competencia y elasticidad del precio
Una vez expira la patente, múltiples fabricantes pueden producir el mismo principio activo.
Esa competencia empuja los precios hacia abajo. En muchos mercados, el precio puede caer 70% o más respecto al innovador.4. Políticas públicas y regulación
Los Estados fomentan el uso de genéricos para controlar el gasto público en salud.
Esto se logra mediante:Listados oficiales de medicamentos esenciales.
Políticas de intercambiabilidad.
Licitaciones públicas basadas en precio y bioequivalencia.
En estos procesos, el incentivo principal es el menor costo unitario.
La reducción del costo inicial de investigación significa que, aunque los medicamentos genéricos tienen el mismo efecto terapéutico que sus equivalentes de marca, generalmente se venden con descuentos sustanciales, alrededor de 50%-80% menos en comparación con el precio del medicamento de marca. Según el IMS Health Institute, los medicamentos genéricos ahorraron $1,67 trillones al sistema de salud estadounidense entre 2007 y 2016.
-
Las principales ventajas de los medicamentos genéricos bioequivalentes son la experiencia de uso en la práctica clínica y el ahorro.
La experiencia de uso en la práctica clínica porque su principio activo lleva años en el mercado. Su menor precio se traduce en un beneficio directo para el ciudadano al pagar menos por el medicamento (el paciente no abandona el tratamiento por una razón económica), al tiempo que contribuyen a racionalizar el gasto público en medicamentos, manteniendo la calidad y la eficacia de la prestación farmacéutica.
-
Si. La Ley 29/2006, del 26 de julio, establece los requisitos de calidad exigibles a los principios activos que se utilizan en la fabricación de medicamentos, que son establecidos mediante el Real Decreto 824/2010, de 25 de junio, por el que se regulan los laboratorios farmacéuticos, los fabricantes de principios activos de uso farmacéutico y el comercio exterior de medicamentos y medicamentos en investigación.
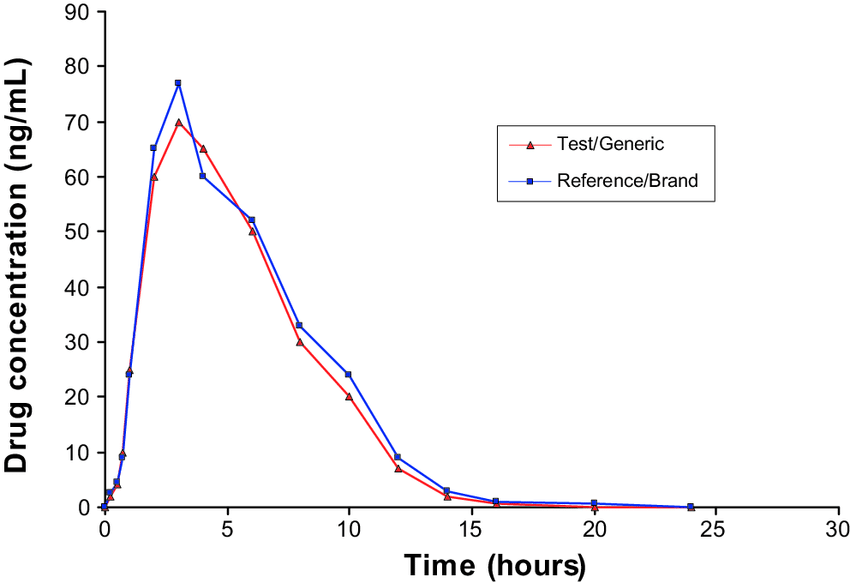

Ejemplo de una gráfica comparativa en un estudio de bioequivalencia. Las líneas de color representan al medicamento original versus un genérico. Una vez ingerido el medicamento y con el paso del tiempo, las concentraciones en sangre inicialmente aumentan, y luego van bajando conforme el medicamento se elimina. Un medicamento bioequivalente debe mostrar curvas similares, e indicadores como Tmax y área bajo la curva al compararse contra el innovador, tal como se muestra en la figura.
